Tengo una pregunta: una vez que tenemos una molécula con los carbonos asimétricos (centros quirales) localizados y representada con la proyección de Fischer, ¿cómo sabemos que va a ser dextrógiro o levógiro? ¿Es el mismo procedimiento que para hallar la configuración R y S?
- - - Actualizado - - -
Creo que se me ha ocurrido una idea con las moléculas del limoneno:
a) Forma R (+)
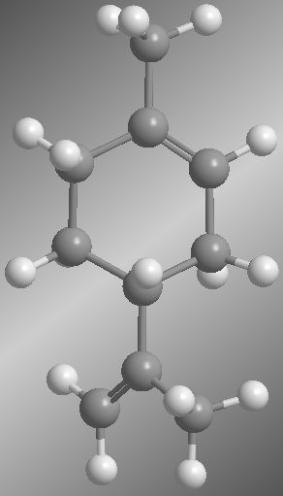
b) Forma (-):
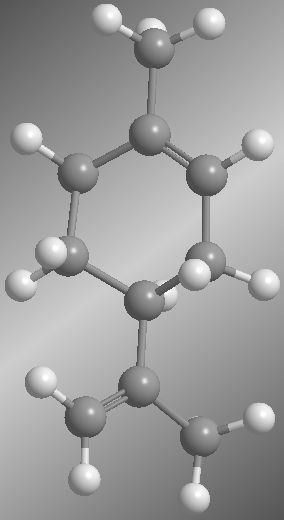
Dibujemos, en cada uno de los casos, los orbitales p que conforman ese doble enlace (enlace ):

Y posteriormente dibujamos el plano que definen estos orbitales:

¿Es eso así o me he pasado de improvisación?
- - - Actualizado - - -
Creo que se me ha ocurrido una idea con las moléculas del limoneno:
a) Forma R (+)

b) Forma (-):

Dibujemos, en cada uno de los casos, los orbitales p que conforman ese doble enlace (enlace ):
Y posteriormente dibujamos el plano que definen estos orbitales:
¿Es eso así o me he pasado de improvisación?






Comentario